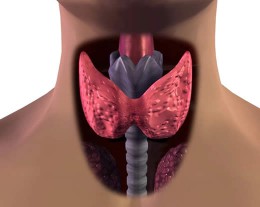
–Ь–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Є–љ—Б—Г–ї–Є–љ–∞

 7550
7550  0
0 –§–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞—В—М –Є —Б–µ–Ї—А–µ—В–Є—А–Њ–≤–∞—В—М –Є–љ—Б—Г–ї–Є–љ —Б —В–µ–Љ, —З—В–Њ–±—Л –µ–≥–Њ –њ–Њ—З—В–Є —Б—А–∞–Ј—Г –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А–Њ–≤–∞—В—М. –°–Ї–Њ—А–µ–µ –Њ—А–≥–∞–љ–Є–Ј–Љ, –Ї–∞–Ї —А–∞—З–Є—В–µ–ї—М–љ–∞—П —Е–Њ–Ј—П–є–Ї–∞ –Ј–∞–њ–∞—Б–∞–µ—В —Н–љ–µ—А–≥–Є—О –≤ —Г–і–Њ–±–љ–Њ–є —Д–Њ—А–Љ–µ, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –њ–Њ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є. –Ш–љ—В–µ—А–µ—Б–љ–Њ, —З—В–Њ —З–µ—А–µ–Ј —Б—Г—В–Ї–Є –≥–Њ–ї–Њ–і–∞–љ–Є—П –≥–ї–Є–Ї–Њ–≥–µ–љ –њ–µ—З–µ–љ–Є –њ–Њ–ї–љ–Њ—Б—В—М—О –Є—Б—З–µ—А–њ–∞–љ –Є –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –≥–ї—О–Ї–Њ–Ј—Л –Ї—А–Њ–≤–Є –Њ—Б—В–∞–µ—В—Б—П –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј [–°–Љ–Є—А–љ–Њ–≤–∞ –Ю.–Ь., 2005]
–Я–Њ–ї–∞–≥–∞–µ–Љ, —З—В–Њ –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є–µ —Б–µ–Ї—А–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —З–µ—А–µ–Ј –њ–Њ—А—В–∞–ї—М–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї —Б–ї—Г–ґ–Є—В, –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ, –і–≤—Г–Љ —Ж–µ–ї—П–Љ: –≤–Њ-–њ–µ—А–≤—Л—Е, —Б–Є–љ—В–µ–Ј—Г –≥–ї–Є–Ї–Њ–≥–µ–љ–∞, –і–µ–њ–Њ–љ–Є—А—Г—П —В–µ–Љ —Б–∞–Љ—Л–Љ –Є–Ј–±—Л—В–Њ–Ї –≥–ї—О–Ї–Њ–Ј—Л; –≤–Њ-–≤—В–Њ—А—Л—Е, —А–µ–≥—Г–ї—П—Ж–Є–Є —Г—А–Њ–≤–љ—П –Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є–Є, –њ—А–µ–њ—П—В—Б—В–≤—Г—П –≥–Є–њ–µ—А–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є–Є. –≠—В—Г –Ј–∞–і–∞—З—Г —А–µ—И–∞–µ—В –Є –ґ–Є—А–Њ–≤–∞—П —В–Ї–∞–љ—М. –£—З–Є—В—Л–≤–∞—П –≤—Л—Б–Њ–Ї—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –∞–і–Є–њ–Њ—Ж–Є—В–Њ–≤, –Њ–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–∞ —Б–≤—П–Ј–∞—В—М –Њ–≥—А–Њ–Љ–љ—Г—О —З–∞—Б—В—М –Є–љ—Б—Г–ї–Є–љ–∞, –і–µ–њ–Њ–љ–Є—А—Г—П –Є–Ј–±—Л—В–Њ–Ї –Љ–∞–Ї—А–Њ—Н—А–≥–Њ–≤ –Є –њ—А–µ–њ—П—В—Б—В–≤—Г—П –µ–≥–Њ –Є–Ј–±—Л—В–Њ—З–љ–Њ–Љ—Г –і–µ–є—Б—В–≤–Є—О –≥–Њ—А–Љ–Њ–љ–∞ –љ–∞ —В–Ї–∞–љ–Є. –Ю–ґ–Є—А–µ–љ–Є–µ —В–µ—Б–љ–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –≥–Є–њ–µ—А–Є–љ—Б—Г–ї–Є–љ–µ–Љ–Є–µ–є –Є, –њ–Њ-–≤–Є–і–Є–Љ–Њ–Љ—Г, –Є–Љ–µ–µ—В –Ј–∞—Й–Є—В–љ—Л–є –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А.
–Ш–љ—Б—Г–ї–Є–љ –њ–Њ—Б–ї–µ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —Б —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤ –њ–µ—А–µ–Љ–µ—Й–∞–µ—В—Б—П –Ї –ї–Є–Ј–Њ—Б–Њ–Љ–∞–Љ, –≥–і–µ –њ–Њ–і–≤–µ—А–≥–∞–µ—В—Б—П –і–µ–є—Б—В–≤–Є—О, –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ, –і–≤—Г—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤. –У–ї—О—В–∞—В–Є–Њ–љ–Є–љ—Б—Г–ї–Є–љ—В—А–∞–љ—Б–≥–Є–і—А–Њ–≥–µ–љ–∞–Ј–∞, —А–∞–Ј—А—Г—И–∞—П –і–Є—Б—Г–ї—М—Д–Є–і–љ—Л–µ –Љ–Њ—Б—В–Є–Ї–Є, –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞–µ—В α- –Є β-—Ж–µ–њ–Є. –¶–Є—В–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–∞—П –Є–љ—Б—Г–ї–Є–љ–Њ–≤–∞—П –њ—А–Њ—В–µ–∞–Ј–∞ –Є–љ–∞–Ї—В–Є–≤–Є—А—Г–µ—В –Є–љ—Б—Г–ї–Є–љ –њ—Г—В–µ–Љ —А–∞–Ј—А—Л–≤–∞ α- –Є β- —Ж–µ–њ–µ–є. –Я–Њ–ї–∞–≥–∞–µ–Љ, —З—В–Њ —А–∞–Ј—А—Г—И–µ–љ–Є–µ –Є–љ—Б—Г–ї–Є–љ–∞ –љ–µ —П–≤–ї—П–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –њ—А–µ—А–Њ–≥–∞—В–Є–≤–Њ–є –≥–µ–њ–∞—В–Њ—Ж–Є—В–Њ–≤, —Н—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤–Њ –≤—Б–µ—Е –Ї–ї–µ—В–Ї–∞—Е.
–Ф–µ–≥—А–∞–і–∞—Ж–Є—П —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ –≥–Њ—А–Љ–Њ–љ–∞ –Є –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є —Д–µ–љ–Њ–Љ–µ–љ —А–µ–≥—Г–ї–Є—А—Г–µ–Љ–Њ–≥–Њ –њ–Њ–љ–Є–ґ–µ–љ–Є—П, –Є–ї–Є down regulation) —П–≤–ї—П—О—В—Б—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–∞–љ–љ—Л–Љ–Є –њ—А–Њ—Ж–µ—Б—Б–∞–Љ–Є. –°—Г—Й–µ—Б—В–≤—Г–µ—В —Б–Њ—Б—В–Њ—П–љ–Є–µ –і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –Љ–µ–ґ–і—Г —Б–Ї–Њ—А–Њ—Б—В—М—О –≤–љ–µ–і—А–µ–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–љ—Л—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–≤, –Є—Е –і–µ–≥—А–∞–і–∞—Ж–Є–µ–є –Є —А–µ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–µ–є, –њ–Њ–≤—В–Њ—А–љ—Л–Љ –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ –≤ —Б—В—А—Г–Ї—В—Г—А—Г –Љ–µ–Љ–±—А–∞–љ—Л, –∞ —В–∞–Ї–ґ–µ —Б–Ї–Њ—А–Њ—Б—В—М—О –Є—Е —Б–Є–љ—В–µ–Ј–∞.
–≠—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —В–µ–Љ —Д–∞–Ї—В–Њ–Љ, —З—В–Њ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Є–љ—Б—Г–ї–Є–љ–∞, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞—П –і–ї—П –љ–∞—З–∞–ї–∞ —Б–љ–Є–ґ–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Њ–±—А–∞—В–љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–∞ –≤–µ–ї–Є—З–Є–љ–µ –Є —Б–Ї–Њ—А–Њ—Б—В–Є –≤–љ–µ–і—А–µ–љ–Є—П –≥–Њ—А–Љ–Њ–љ–∞ –≤ –Ї–ї–µ—В–Ї—Г; –њ—А–Є —Г—Б–ї–Њ–≤–Є—П—Е, –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Б–Ї–Њ—А–Њ—Б—В—М –њ–Є–љ–Њ—Ж–Є—В–Њ–Ј–∞ –≤ –Ї–ї–µ—В–Ї–µ.
–Ю–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ —Н—А–Є—В—А–Њ—Ж–Є—В—Л —Б–њ–Њ—Б–Њ–±–љ—Л –љ–∞–Ї–∞–њ–ї–Є–≤–∞—В—М –Є —В—А–∞–љ—Б–њ–Њ—А—В–Є—А–Њ–≤–∞—В—М –Є–љ—Б—Г–ї–Є–љ [–°–∞–љ–і—Г–ї—П–Ї –Ы.–Ш.,1987]. –°–≤—П–Ј—Л–≤–∞—П –Є–Ј–±—Л—В–Њ–Ї –Є–љ—Б—Г–ї–Є–љ–∞ –Є –Њ—В–і–∞–≤–∞—П –µ–≥–Њ –њ—А–Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є, —Н—А–Є—В—А–Њ—Ж–Є—В—Л —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—В –∞–Ї—В–Є–≤–љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –≥–Њ—А–Љ–Њ–љ–∞, —Б–≥–ї–∞–ґ–Є–≤–∞—О—В —А–µ–Ј–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –µ–µ –њ—А–Є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–і–≤–Є–≥–∞—Е —Б–µ–Ї—А–µ—Ж–Є–Є –Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞.
–Т —В–∞–Ї–Њ–є –ґ–µ –Љ–µ—А–µ –Є–љ—Б—Г–ї–Є–љ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П –Є —Б —Н–љ–і–Њ—В–µ–ї–Є–Њ—Ж–Є—В–∞–Љ–Є, –≤—Л–Ј—Л–≤–∞—П –Є—Е –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О. –≠–љ–і–Њ—В–µ–ї–Є–Њ—Ж–Є—В—Л –љ–∞–Є–±–Њ–ї–µ–µ —Г—П–Ј–≤–Є–Љ—Л –і–ї—П —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –љ–∞—Е–Њ–і—П—Й–Є—Е—Б—П –≤ —Б–Є—Б—В–µ–Љ–љ–Њ–Љ –Є —В–Ї–∞–љ–µ–≤–Њ–Љ –Ї—А–Њ–≤–Њ—В–Њ–Ї–µ –≤ —Б–≤—П–Ј–Є —Б –Є—Е —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–µ–Љ –љ–∞ –≥—А–∞–љ–Є—Ж–µ –Љ–µ–ґ–і—Г —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–µ–є –Ї—А–Њ–≤—М—О –Є —В–Ї–∞–љ—П–Љ–Є. –≠–љ–і–Њ—В–µ–ї–Є–Њ—Ж–Є—В—Л –Њ–±–ї–∞–і–∞—О—В –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Є —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О.
–Ю–Ї–Њ–ї–Њ 40% –Є–љ—Б—Г–ї–Є–љ–∞ (–њ–Њ –і–∞–љ–љ—Л–Љ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –∞–≤—В–Њ—А–Њ–≤, 15-20%) –Є–љ–∞–Ї—В–Є–≤–Є—А—Г–µ—В—Б—П –њ–Њ—З–Ї–∞–Љ–Є. –У–Њ—А–Љ–Њ–љ —Д–Є–ї—М—В—А—Г–µ—В—Б—П –≤ –Ї–ї—Г–±–Њ—З–Ї–∞—Е, –∞ –≤ –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е –Ї–∞–љ–∞–ї—М—Ж–∞—Е –њ–Њ—З—В–Є –њ–Њ–ї–љ–Њ—Б—В—М—О —А–µ–∞–±—Б–Њ—А–±–Є—А—Г–µ—В—Б—П –Є —А–∞–Ј—А—Г—И–∞–µ—В—Б—П –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ–Є —Д–µ—А–Љ–µ–љ—В–∞–Љ–Є. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ—А–Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –њ–Њ–≥–ї–Њ—Й–µ–љ–Є–µ –Є –і–µ–≥—А–∞–і–∞—Ж–Є—П –Є–љ—Б—Г–ї–Є–љ–∞ –њ–Њ—З–Ї–∞–Љ–Є —Г–Љ–µ–љ—М—И–∞—О—В—Б—П –і–Њ 9-10%, –њ–Њ—Н—В–Њ–Љ—Г —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –њ—А–Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –Є–љ—Б—Г–ї–Є–љ–µ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П.
–†–Њ–ї—М –њ–Њ—З–µ–Ї –≤ –Є–љ–∞–Ї—В–Є–≤–∞—Ж–Є–Є —Н–Ї–Ј–Њ–≥–µ–љ–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –≤–µ–ї–Є–Ї–∞, —В–∞–Ї –Ї–∞–Ї, –≤—Б–∞—Б—Л–≤–∞—П—Б—М –Є–Ј –Љ–µ—Б—В–∞ –Є–љ—К–µ–Ї—Ж–Є–Є, –Є–љ—Б—Г–ї–Є–љ –њ–Њ–њ–∞–і–∞–µ—В –≤ –±–Њ–ї—М—И–Њ–є –Ї—А—Г–≥ –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –Є –њ–Њ—З–Ї–Є, –∞ —Н–љ–і–Њ–≥–µ–љ–љ—Л–є –Є–љ—Б—Г–ї–Є–љ —Б–љ–∞—З–∞–ї–∞ –њ–Њ—Б—В—Г–њ–∞–µ—В –≤ –њ–µ—З–µ–љ—М –Є –ї–Є—И—М –Ј–∞—В–µ–Љ –Љ–µ–љ—М—И–∞—П –µ–≥–Њ —З–∞—Б—В—М – –≤ –±–Њ–ї—М—И–Њ–є –Ї—А—Г–≥ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є –њ–Њ—З–Ї–Є. –Т –њ–Њ—З–Ї–∞—Е –Є–љ—Б—Г–ї–Є–љ —Д–Є–ї—М—В—А—Г–µ—В—Б—П –≤ –Ї–ї—Г–±–Њ—З–Ї–∞—Е, –∞ –≤ –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е –Ї–∞–љ–∞–ї—М—Ж–∞—Е –њ–Њ—З—В–Є –њ–Њ–ї–љ–Њ—Б—В—М—О —А–µ–∞–±—Б–Њ—А–±–Є—А—Г–µ—В—Б—П –Є —А–∞–Ј—А—Г—И–∞–µ—В—Б—П –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ–Є —Д–µ—А–Љ–µ–љ—В–∞–Љ–Є, –њ—А–Є—З–µ–Љ —Н–љ–і–Њ—Б–Њ–Љ–∞–ї—М–љ–Њ-–ї–Є–Ј–Њ—Б–Њ–Љ–∞–ї—М–љ—Л–є –њ—Г—В—М –Є–љ–∞–Ї—В–Є–≤–∞—Ж–Є–Є –Є–љ—Б—Г–ї–Є–љ–∞ –≤ –њ–Њ—З–µ—З–љ—Л—Е –Ї–∞–љ–∞–ї—М—Ж–∞—Е –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В.

–°–≤–µ–ґ–Є–µ —Б—В–∞—В—М–Є
- –Ъ—Г–њ–Є—В—М Freestyle Libre
- –Ь–Њ–ґ–љ–Њ –ї–Є –Ј–∞–Љ–µ–љ–Є—В—М —Г–Ї–Њ–ї—Л –љ–µ–Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ–Є —Б–њ–Њ—Б–Њ–±–∞–Љ–Є –≤–≤–µ–і–µ–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–∞ –Є –≥–ї—О–Ї–Њ–Љ–µ—В—А–Є–Є?
- –Э–µ–Њ–љ–∞—В–∞–ї—М–љ—Л–є —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В
- –Ы–Є–њ–Њ–∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–є —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В
- –І—В–Њ —В–∞–Ї–Њ–µ –њ—А–µ–і–Є–∞–±–µ—В –Є –њ–Њ—З–µ–Љ—Г –Њ–љ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В?
–І–Є—В–∞–є—В–µ —В–∞–Ї–ґ–µ:

 –Ш–љ—Б—Г–ї–Є–љ
–Ш–љ—Б—Г–ї–Є–љ 27.01.2014
27.01.2014